Anvisa recusa uso emergencial de Coronavac para crianças de 3 a 17 anos
Previsão de Mato Grosso do Sul é que uso permitiria vacinar adolescentes e angariar mais doses para reforço

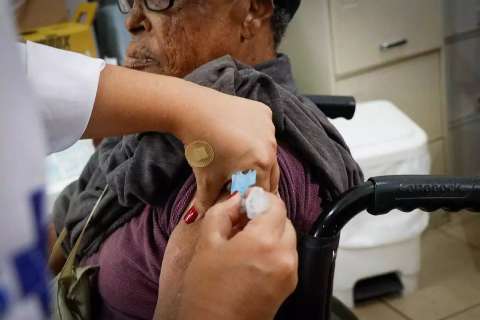
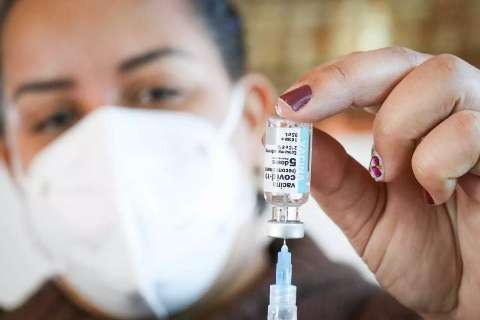
Anvisa (Agência Nacional de Vigilância Sanitária) não liberou o uso emergencial das vacinas contra a covid-19, da Coronavac, para pessoas de três a 17 anos, em reunião feita na tarde desta quarta-feira (18).
O Instituto Butantan, que fabrica os imunizantes que deram início à campanha de imunização contra o coronavírus, no começo de janeiro, solicitou a expansão dessa utilização, que foi negada por todos os diretores do órgão. Ainda assim, foi destacado que o uso em adultos segue permitido, já que cumpre requisitos de exigência e tem sido essencial para a redução de casos da doença.
A expectativa da SES (Secretaria Estadual de Saúde), nesta semana, era de que essa patente fosse liberada a essa faixa etária.
Em coletiva feita na terça-feira (17), o secretário estadual de Saúde, Geraldo Resende, disse que caso fossem liberadas, elas poderiam dar continuidade a vacinação de adolescentes, de modo a liberar vacinas para outras finalidades, tais como a aplicação de uma "terceira dose" a idosos com comorbidades.
Critérios - Em geral, a vacina sino-brasileira foi elogiada pelos técnicos da Anvisa, que analisaram dados fornecidos pelo Butantan, mas por conta da falta de evidências mais concretas da proteção verificada em população pediátrica, houve a recusa.
A conclusão de um dos fiscais, Gustavo Mendes Lima Santos, é de que é impossível estimar se, a partir dos anticorpos gerados nos indivíduos analisados, se há uma imunidade suficiente para reduzir a chance de casos graves.
"Não é conhecida qual a eficácia ou capacidade de indução de resposta imune pela vacina em crianças com comorbidades e imunossuprimidas, mais vulneráveis a casos graves", disse avaliação feita pela Agência.