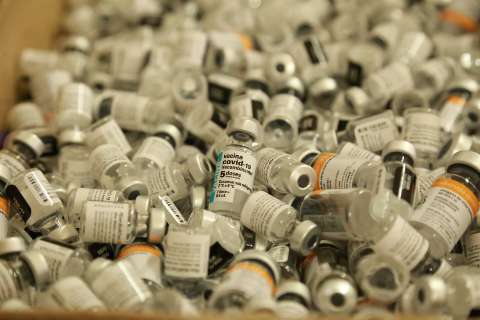
Lote recolhido da Coronavac em MS não provocou efeitos adversos
Estado recebeu 800 doses de lote interditado e aplicou 732, sobrando 68 para devolução à Anvisa
As pessoas que receberam doses da vacina Coronavac/Butantan que devem ser recolhidas por determinação da Anvisa (Agência Nacional de Vigilância Sanitária) estão sendo acompanhadas pela SES (Secretaria de Estado de Saúde) e até o momento, nenhuma delas apresentou qualquer reação adversa.
Em nota, a secretaria informou que “nenhuma das pessoas que tomou vacinas deste lote apresentaram reações adversas graves”, citando o lote L202106038, que é um dos que teve o recolhimento determinado pela agência.
Mato Grosso do Sul recebeu 800 doses dele e aplicou 732, sobrando 68 para devolução à agência, que identificou que o envase na vacina, feito em laboratório na China, não seguiu condições satisfatórias de Boas Práticas de Fabricação conforme estabelecido pelo órgão brasileiro.
A SES informou ainda que essas doses foram recebidas em 27 de julho e na época, foram distribuídas para os 13 polos de saúde indígena de Mato Grosso do Sul. “Em 6 de setembro a Anvisa determinou a suspensão da aplicação das doses do lote. A Secretaria de Estado de Saúde na ocasião imediatamente pediu aos municípios o recolhimento dessas doses”, diz a nota.
Há algumas semanas, o Campo Grande News já havia identificado que 509 pessoas se vacinaram com doses do lote recolhido, mas na ocasião, os dados eram de planilhas do Ministério da Saúde. Agora, os dados oficiais mostram que 732 doses foram aplicadas.
Histórico - no dia 3 de setembro de 2021, a Anvisa foi comunicada pelo Instituto Butantan que o seu parceiro Sinovac, fabricante da vacina CoronaVac, havia enviado para o Brasil 25 lotes na apresentação frasco-ampola (monodose e duas doses), totalizando 12.113.934 doses, que foram envasados em instalações não inspecionadas pela Anvisa. A unidade fabril responsável pelo envase não foi objeto de avaliação da Agência quando da aprovação da AUE da vacina CoronaVac.
Diante das informações apresentadas pelo Instituto Butantan, e considerando as características do produto e a complexidade do processo fabril, já que vacinas são produtos estéreis (injetáveis) que devem ser fabricados em rigorosas condições assépticas, bem como o desconhecimento pela Anvisa sobre o cumprimento das Boas Práticas de Fabricação (BPF) por parte da empresa, a Agência, no estrito cumprimento de sua missão institucional, entendeu necessária a adoção de medida cautelar com o propósito de mitigar um potencial risco sanitário.
Assim, foi publicada a Resolução (RE) 3.425, que determinou a interdição cautelar e proibiu a distribuição e o uso dos lotes envasados na planta não aprovada na AUE.