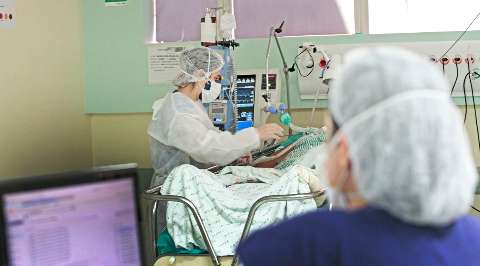
Anvisa estabelece medidas para evitar desabastecimento na pandemia
Regras valem para aquisição de medicamentos, oxigênio e dispositivos médicos já em falta no mercado
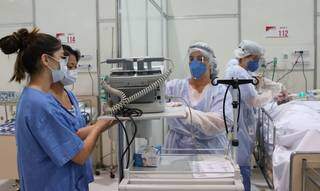
Diante dos leitos de covid-19 lotados, a Anvisa (Agência Nacional de Vigilância Sanitária) publicou, na noite desta sexta-feira (19), quatro medidas para evitar o desabastecimento de medicamentos, oxigênio e dispositivos médicos utilizados no país no enfrentamento da pandemia de Covid-19.
As regras têm como objetivo facilitar processos de distribuição de medicamentos e importação de dispositivos médicos e medicamentos prioritários para uso em serviços de saúde. Aplica ainda excepcionalidades temporárias a requisitos para a utilização de cilindros de oxigênio na área da saúde pública.
Em Mato Grosso do Sul, não há mais leitos de UTI (Unidade de Terapia Intensiva) para atender pacientes com covid-19. O colapso já impacta no estoque de medicamentos e também dificulta a compra, pois, com a alta demanda do mercado, fornecedores elevaram os preços em 250% a 300%, conforme o MPMS (Ministério Público de Mato Grosso do Sul).
Nesta semana, o Simed-MS (Sindicato dos Médicos de Mato Grosso do Sul) emitiu alerta de sobrecarga da rede de oxigênio do HRMS (Hospital Regional de Mato Grosso do Sul), unidade de referência no tratamento da covid-19.
Confira as novas regras estabelecidas para aquisição dos insumos e medicamentos:
Registro - A primeira medida (Resolução da Diretoria Colegiada (RDC) nº 484/2021) diz respeito ao registro de medicamentos utilizados para intubação. Esses medicamentos poderão ser comercializados excepcionalmente apenas com notificação à Anvisa. Anestésicos, sedativos, bloqueadores neuromusculares e outros medicamentos hospitalares usados para manutenção da vida de pacientes estão nessa lista.
Distribuição - A Anvisa facilitou também o processo de distribuição de medicamentos estéreis (injetáveis). A medida permite que a carga do medicamento possa ser transportada às distribuidoras e instituições de saúde enquanto as empresas realizam os testes de controle de qualidade. O medicamento, porém, só pode ser utilizado após o fabricante comunicar sobre a aprovação do produto nos testes de esterilidade, no tempo de 7 dias de incubação.
Importação - A Agência simplificou os processos de importação de dispositivos médicos e medicamentos prioritários para uso em serviços de saúde. A Resolução da Diretoria Colegiada (RDC) nº 483/2021 possibilita a importação direta de um rol de medicamentos e dispositivos médicos, não regularizados no país, em caráter excepcional e temporário por órgãos e entidades públicas e privadas, bem como serviços de saúde.
Oxigênio medicinal - Já a Resolução da Diretoria Colegiada (RDC) nº 482/2021 aplica excepcionalidades temporárias a requisitos para a utilização de cilindros de oxigênio na área da saúde pública. As medidas se referem à utilização de cilindros de oxigênio não medicinal, utilização de rampas de enchimento de cilindros industriais para o enchimento de cilindros medicinais e utilização de unidades de envasamento exclusivo de gases industriais para o envasamento de gases medicinais.
O objetivo da resolução é proporcionar o aumento da oferta e abastecimento de oxigênio medicinal.